近日,一區(qū)top期刊《Genes & Diseases》(IF=7.243)在線發(fā)表了重慶醫(yī)科大學附屬第一醫(yī)院骨科黃偉教授團隊題為“The miR-21-5p enriched in the apoptotic bodies of M2 macrophage-derived extracellular vesicles alleviates osteoarthritis by changing macrophage phenotype” 的研究論文��,首次證明替代激活的M2-Mφ凋亡小體可通過誘導經(jīng)典激活的M1-Mφ向M2樣表型轉化而減輕骨關節(jié)炎(OA)的進展����,為與促炎和抗炎免疫反應失衡相關的各種疾病提供一種新的治療策略。


文獻鏈接:https://doi.org/10.1016/j.gendis.2022.09.010
巨噬細胞(Mφs)是一種天然免疫細胞��,由特定微環(huán)境信號激活可極化為經(jīng)典活化(M1-M?s)和交替活化(M2-M?s)兩種表型�,分別表現(xiàn)為促炎和抗炎作用。這兩種亞型之間的平衡對炎癥性疾病的進展和預后至關重要��。研究表明�����,在M1-M?占主導地位����,會引起OA的發(fā)生發(fā)展,而將促炎的M1-Mφ重新編程為抗炎的M2-Mφ�����,可以減輕OA模型的滑膜炎癥和軟骨破壞。巨噬細胞表型的維持受遺傳和表觀遺傳信號驅動�,并受環(huán)境信號的影響,這為調節(jié)巨噬細胞的極化�����,用于預防或治療OA提供了一種可能有效的治療方法�����。
凋亡小體(ABS)是程序性凋亡的產(chǎn)物�����,可通過巨噬細胞表面的“Eat-me”信號(鈣網(wǎng)織蛋白)被巨噬細胞特異性識別����。以前的研究已經(jīng)觀察到��,巨噬細胞對凋亡細胞(凋亡小體)的內(nèi)吞有助于組織修復和炎癥的消退�。這種炎癥的減輕和組織修復的增強是否與巨噬細胞攝取凋亡小體后的表型變化有關尚不清楚,凋亡小體發(fā)揮的功能也有待進一步研究��。
基于上述背景����,黃偉教授團隊開展了M2-M?s衍生的凋亡小體(M2-ABs)在調節(jié)小鼠OA模型巨噬細胞M1/M2平衡中的作用研究��。數(shù)據(jù)顯示�,M2-ABS可以被M1-M?s靶向攝取�,并在24小時內(nèi)將M1表型重新編程為M2。M2-ABS顯著改善了小鼠OA的嚴重程度�����,減輕了M1介導的促炎環(huán)境�,并抑制了軟骨細胞的凋亡。RNA-SEQ顯示M2-ABS富含miR-21-5p�����,miR-21-5p是一種與關節(jié)軟骨退變負相關的微小RNA�。抑制M1-M?中miR-21-5p的功能顯著減少了體外細胞轉染M2-ABS后引導的M1向M2的重編程。
綜上所述�����,這些結果表明M2來源的M2-ABs可以通過逆轉M1巨噬細胞引起的炎癥反應來防止關節(jié)軟骨損傷并改善OA小鼠的步態(tài)異常��。其機制可能與miR-21-5p調節(jié)抑制炎癥因子有關。M2-ABs的應用可能代表了一種新的細胞療法�����,并可能為治療OA或慢性炎癥提供一種有價值的策略��。
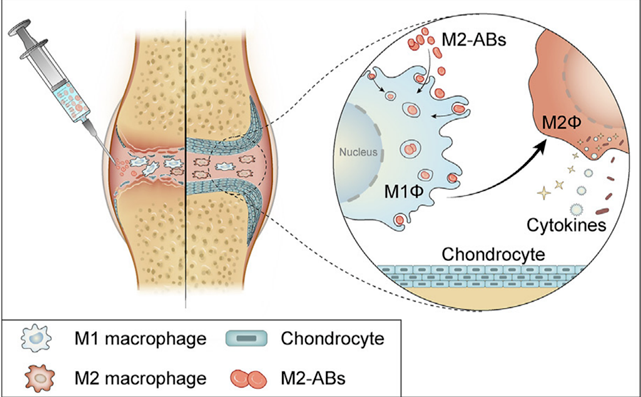
△ 圖1
凋亡小體引導的巨噬細胞重編程示意圖
來源于M2-Mφ的凋亡小體(M2-ABs)可觸發(fā)M1向M2轉化���,從而減緩骨性關節(jié)炎的進展
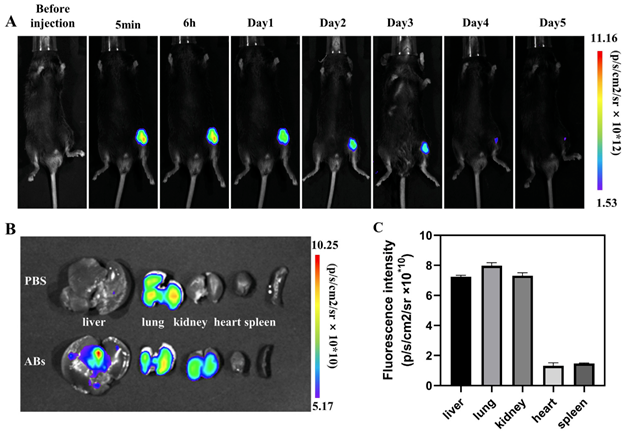
研究中����,在觀察M2-ABs在體內(nèi)的生物分布時����,使用了AniView系列多模式動物活體成像系統(tǒng)進行拍攝�。
△ 圖2
(A)、Cy7NHS標記的M2-ABs實時體內(nèi)成像�����。在膝關節(jié)注射磷酸鹽緩沖鹽水和50μg/μl的M2-ABs后�,在指定的時間進行成像
(B)、小鼠服用M2-ABs第3天后的主要器官的體外成像
(C)����、膝關節(jié)注射Cy7-NHS標記的M2-ABs第3天后的內(nèi)臟熒光分布統(tǒng)計